【临床数据首发】天然小分子创新药注射用绿原
【临床I期试验设计】
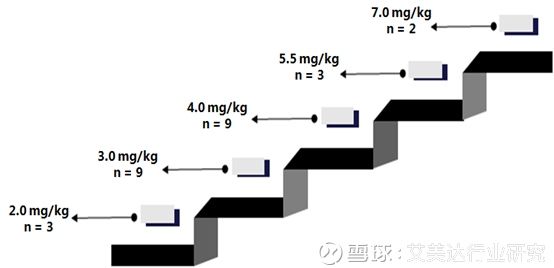
受试人群:经标准治疗失败的复发性高级别脑胶质瘤患者
研究目的:确定MTD和DLT、药代动力学特征、初步观察疗效
给药方案:肌肉注射,1次/天,28天/周期
入组人数:26例(IV级21例;III级5例)
【临床I期-入组受试者基线特征】
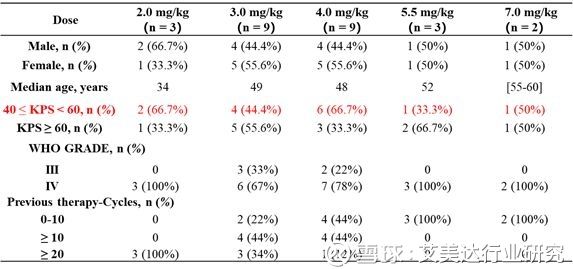
本次试验入组受试者均为经标准方案治疗后疾病进展的高级别恶性脑胶质瘤患者;入组的26例受试者中有14例KPS评分小于60分(其中50%受试者KPS评分为40分)。
【临床I期安全性数据】
不良事件
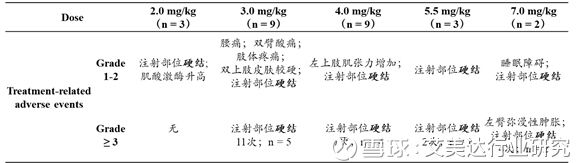
与药物相关的不良事件主要为注射部位的肌肉硬结,无其它毒副作用,绿原酸安全性良好。
7.0 mg/kg 为 DLT;5.5mg/kg 为MTD。
I期数据显示,除出现剂量限制性毒性(DLT)组外,95%的受试者在出现肌肉硬结后能继续给药并完成既定的给药计划,用药依从性良好。???
【临床I期-各剂量组药代动力学数据】
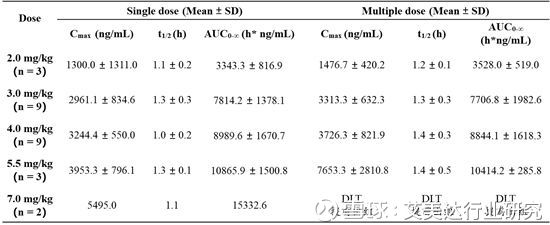
在人体内血药浓度呈剂量依赖性特征,药物代谢和排泄速率较快,无蓄积毒性(t1/2)。
绿原酸药代动力学特征符合天然小分子免疫药物的代谢特点。
【临床I期有效性评价-中位OS】
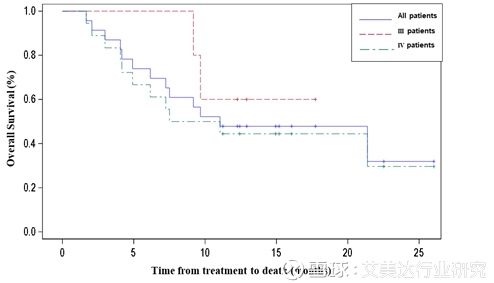
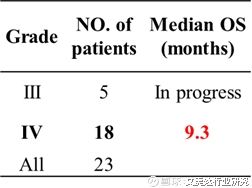
以随机用药作为起点计算,其中IV级人群中位OS为9.3个月(文献记录多次复发性GBM受试者中位OS仅有3-4.6个月),提高了2-3.1倍。
截止到2018年09月10日,以随机用药作为起点计算,本次试验IV级人群最长生存时间达30个月(0001号)。
【临床I期有效性评价-中位OS(3 mg/kg组)】
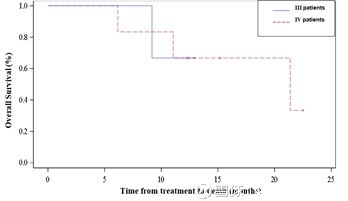
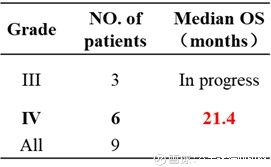
I期推荐剂量为 3.0 mg/kg(共9例,其中III级3人,IV级6人)。
以随机用药作为起点计算,该组IV级人群中位OS达21.4个月(文献记录多次复发性GBM受试者中位OS仅有3-4.6个月),提高了4.7-7.1倍。
截止到2018年09月10日,以随机用药作为起点计算,有效剂量组IV级人群最长生存时间达25.8个月(0005号)。
【临床I期探索性研究数据】
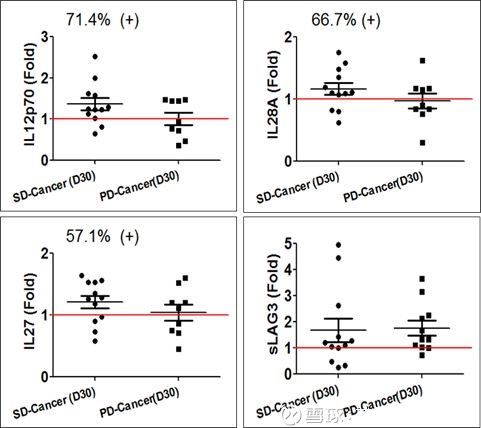
入组受试者26例,3例提前出组。
1个月的DCR为52.17%;2个月的DCR为33.33%。
部分免疫指标(IL12P70、IL28A、IL27)与受试者的疾病控制(SD人群)呈正相关性。
sLAG3有待下阶段临床试验中扩大受试人群进一步验证其与疗效的相关性。
【受试者愈后与免疫指标的相关性数据】
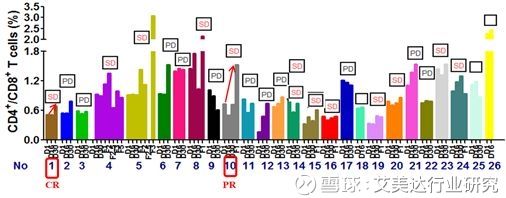
根据肿瘤评估RANO标准,后期生存期随访中出现1例完全缓解(CR),1例部分缓解(PR)受试者均在使用绿原酸超8个月后出现的疾病缓解现象。2例受试者愈后与免疫指标(CD4+/CD8+)的变化呈正相关。